Você está na sessão de Leucemia Mieloide Crônica, para ver sobre outras Leucemias CLIQUE AQUI
Última atualização em 18 de fevereiro de 2025
QUAIS EXAMES SÃO UTILIZADOS NO DIAGNÓSTICO DA LEUCEMIA MIELOIDE CRÔNICA?
Como muitas pessoas com LMC não apresentam sintomas, o diagnóstico da Leucemia Mieloide Crônica muitas vezes acontece apenas quando, em exames de rotina, um número muito alto de glóbulos brancos são detectados no sangue.
O diagnóstico definitivo da LMC inclui estudos nas células do sangue e da medula óssea. O hematologista e o patologista são os médicos especialistas capacitados para identificar doenças, estudando as células do sangue e da medula óssea com um microscópio.
O conjunto de exames para diagnosticar a LMC é:
LEUCEMIA MIELOIDE CRÔNICA HEMOGRAMA
O Hemograma completo com contagem diferencial é usado para medir o número de glóbulos brancos, glóbulos vermelhos e plaquetas em uma amostra de sangue. Também mede a quantidade de hemoglobina dentro das células vermelhas e a porcentagem de glóbulos vermelhos na amostra. O hemograma completo deve incluir a contagem diferencial dos diferentes tipos de glóbulos brancos. Pessoas com LMC costumam ter:
- Aumento na contagem dos glóbulos brancos, muitas vezes a níveis muito altos
- Redução na contagem dos glóbulos vermelhos
- Possível redução ou aumento no número de plaquetas, dependendo da gravidade da LMC
ESFREGAÇO PERIFÉRICO
As células do sangue são colocadas em uma lâmina, tingidas e examinadas com um microscópio. Este exame mostra:
- O número, tamanho, forma e tipo das células sanguíneas
- A forma específica dos glóbulos brancos
- A proporção de células imaturas (blastos) comparadas com a proporção de células amadurecendo e glóbulos brancos totalmente maduros. Os blastos não devem estar presentes no sangue de pessoas saudáveis.
ASPIRADO E BIÓPSIA DA MEDULA ÓSSEA
Esses exames são usados para examinar as células da medula óssea em busca de anormalidades. Normalmente a coleta dos dois exames é feita ao mesmo tempo. O hematologista faz uma anestesia local no osso do quadril do paciente para que ele não sinta dor. Para fazer a aspiração da medula óssea (mielograma), uma agulha oca é inserida no osso do quadril até a medula óssea e coleta-se uma amostra de sangue com as células. Para a biópsia da medula óssea, uma agulha mais larga é usada para remover um pequeno pedaço de osso que contenha medula óssea. Ambas as amostras são examinadas em um microscópio para procurar células doentes.
ANÁLISE CITOGENÉTICA
Citogenética é o estudo dos cromossomos e suas possíveis anormalidades. Amostras da medula óssea são examinados em um microscópio para encontrar mutações cromossômicas como as do cromossomo Philadelphia (Ph). A presença do cromossomo Ph na medula óssea, juntamente com o aumento da contagem dos glóbulos brancos e outros achados característicos do hemograma e da medula óssea confirmam o diagnóstico de LMC. Como já comentado, uma pequena porcentagem das pessoas que tem LMC não apresentam o cromossomo Ph detectável por citogenética, mas quase sempre eles têm um teste positivo para a fusão do gene BCR-ABL no cromossomo 22 por meio de outros tipos de exames.
PCR - REAÇÃO EM CADEIA DA POLIMERASE QUANTITATIVA
O que é PCR?
Exame PCR é o teste mais sensível para detectar e medir a quantidade de genes BCR-ABL na amostra de sangue ou de medula óssea. Pode detectar quantidades muito pequenas do gene BCR-ABL, mesmo quando o cromossomo Ph não pode ser detectado pelo teste de citogenética. O nível de sensibilidade deste exame é alto, uma vez que pode detectar uma célula de LMC em uma quantidade de 100.000 a 1.000.000 de células normais. A contagem das células do sangue, exames de medula óssea, FISH e PCR exame também podem ser usados para medir como a pessoa está reagindo ao tratamento depois que ele já tiver começado. É recomendado fazer o exame de sangue PCR a cada 3 meses durante os primeiros 2 anos de tratamento. Depois de 2 anos, se o paciente estiver reagindo bem, o teste deve ser feito a cada 6 meses.
EXAME FISH (HIBRIDIZAÇÃO IN SITU FLUORESCENTE)
FISH é um exame laboratorial usado para examinar genes e cromossomos nas células. O FISH é um método mais sensível para detectar o cromossomo Ph do que testes normais de citogenética e pode identificar a presença do gene BCR-ABL (veja figura 4). No caso da LMC, o FISH usa sondas de cor que se ligam a segmentos específicos do DNA dos genes BCR e ABL nos cromossomos. Os genes BCR e ABL são marcados com diferentes substâncias químicas, cada uma das quais libera uma cor diferente, permitindo sua identificação. A cor aparece no cromossomo que contém o gene, isto é, no cromossomo 9 para ABL e no cromossomo 22 para BCR e, portanto, pode detectar o pedaço do cromossomo 9 que se moveu para o cromossomo 22 nas células de LMC. A fusão do gene BCR-ABL é mostrada pela sobreposição de cores nas duas sondas. A figura abaixo mostra o momento em que o Gene BCR-ABL está sendo identificado nas células, usando o FISH.
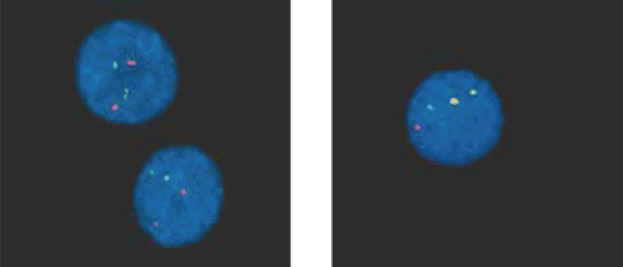
Hibridização in situ fluorescente, ou FISH, é um método de teste que usa moléculas fluorescentes para marcar o gene BCR-ABL na LMC. Nas células normais, dois sinais vermelhos e dois verdes indicam a localização normal do gene ABL e BCR, respectivamente. Nas células anormais, a fusão BCR-ABL é visualizada por meio da fusão dos sinais verde e vermelho. É frequentemente detectado como amarelo fluorescente (mostrado por setas).
Análise da mutação do gene BCR-ABL
Algumas vezes, ocorrem mutações no gene BCR-ABL que produz a proteína BCR-ABL. Essas mutações alteram a forma da proteína BCR-ABL, podendo afetar como os inibidores de tirosina quinase ligam-se à proteína BCR-ABL para bloquear os sinais de crescimento.
A análise da mutação genética BCR-ABL é um teste que procura por mutações nesse gene que podem fazer com que certos inibidores de tirosina quinase parem de funcionar.
O teste da mutação do gene BCR-ABL deve ser realizado em caso de:
- Resposta inadequada a terapia inicial com inibidores de tirosina quinase
- Falha em cumprir a meta do tratamento
- Perda de resposta hematológica, citogenética, aumento de 1 log nos níveis de BCR-ABL ou a perda da resposta molecular maior
- Progressão para a fase acelerada ou blástica
- Uma análise de mutação não precisa ser feita em pacientes que estejam trocando de medicamento devido a efeitos colaterais.